2012年1月12日に維持透析患者のための簡易栄養スクリーニングツールを掲載しましたが,その参照文献の一つを読んだので訳してみました.MISという栄養評価法はSGAから発展したDMSをさらに発展させたもので,入院頻度,在院日数,入院までの期間及び死亡率と有意に相関するというのが論旨です.日本語訳の瑕疵の責任は私にあります.
低栄養炎症スコアは維持透析患者の罹患率と死亡率とに相関する
Kamyar Kalantar-Zadeh, MD, Joel D. Kopple, MD, Gladys Block, PhD, and Michael H. Humphreys, MD
American Journal of Kidney Diseases, Vol 38, No 6 (December), 2001: pp 1251-1263
Malnutrition inflammation complex syndrome (MICS) は維持透析患者において一般的に起こる合併症であり,罹患率と死亡率の増加に相関すると思われる.最適で総合的で定量的なシステム,MICS を評価するシステムは臨床状態の有用な指標となりうるし,維持透析患者の予後を予見しうるかもしれない.それ故,将来の入院や死亡率などと同様に,従来の栄養と炎症の指標を比較して我々はそのような装置を開発し検証しようとした.従来の Subjective Global Assessment (SGA) の要素を用いて,3段階の半定量的な点数,Dialysis Malnutrition Score (DMS), SGA 要素の7つを含み,総点数が7点(正常)から35点(重症低栄養)の範囲になる完全に定量的な採点システムは最近開発されたものである.DMS を改善するため,我々は3つの新しい要素を7つの DMS の要素に追加した.Body mass index と血清アルブミンと血清トランスフェリンレベルを示す TIBC である.この新しく総合的な Malnutrition-inflammation score (MIS) は10の要素を持ち,それぞれが0(正常)から3(非常に重度)までの4段階の重症度を持つ.MIS の10個の要素の合計点素は0点から30点の範囲であり,点数の増加は重症度の増加を示している.これらの点数を身体測定,近赤外線で測定した体脂肪率,血清CRPを含む採血検査,12ヶ月間の前向き入院及び死亡率と比較した.少なくとも3ヶ月経過した83名の維持透析外来患者(男性44名,女性39名,年齢は59±15歳)が研究の最初に検証され,1年間フォローした.熟練した医師がすべての患者に同時に SGA, DMS, MIS を評価した.症例を混合して調整した相関係数は在院日数と有意 (r = 0.45; P < 0.001) であり,入院頻度とも有意 (r = 0.46, P < 0.001) であった.SGA や DMS と比較して,MIS では最も適切な相関係数はより強かった.MIS では,SGA や DMS ではなく,クレアチニン,ヘマトクリット,CRPレベルと相関した.12ヶ月間の観察期間中,9名の患者が死亡し6名が研究から離脱した.コックス比例ハザードモデルで計算した相対死亡危険度は MIS が10点増加するごとに10.43上昇した(95%信頼区間2.28から47.64; P= 0.002).MIS はその要素や予測死亡率の異なるサブバージョンに優れていた.MIS は透析患者の栄養や炎症や貧血等と同様,将来の入院や死亡率と強く相関する総合的な採点システムだと分かった.MIS は個々の検査値同様,透析の予後予測因子として,また MICS の指標として従来の SGA や DMS よりも優れている可能性がある.
2001 by the National Kidney Foundation, Inc.
INDEX WORDS: Dialysis; malnutrition; inflammation; nutritional assessment; hospitalization; mortality; near infrared; albumin; transferrin; C-reactive protein (CRP).
維持透析を受けている末期腎不全患者には蛋白質エネルギー低栄養と炎症の両者を合併する率が高い.これらの観察は異なる研究班によって繰り返しなされてきているが,低栄養炎症混合症候群 (MICS) なる造語を作り出すに至った.蛋白質エネルギー低栄養をもたらす因子と炎症性サイトカインは,それ自身が食欲不振や筋萎縮,低アルブミン血症,不応性貧血,また恐らく動脈硬化の原因にもなっており,明らかに MICS の原因である.MICS の幾つかの機能は単独でも複数でも,これらの患者においては罹患率や死亡率同様,疾患の程度の強い予測因子である.
多くの低栄養や炎症の検査が臨床的予後と相関するにもかかわらず,これらの値は一般には個々の患者の組み合わせ方法のために臨床状態や予後を検証しない.ごく少数の低栄養や炎症の計測がこれらの臨床状態の全体的な評価を与えるにすぎない.面倒な方法や高度な計算が不要で,実用的で簡単なツールであれば,仮に最適な管理のために定量的方法で末期腎不全患者をリスク層別化できるなら,総合的採点システムがこの目的に有用である可能性がある. それゆえ我々は,総合的で半定量的だが使いやすい,末期腎不全患者の評価のための採点システムを開発しようとした.この報告はこのようなシステムについて述べ,従来の栄養状態,炎症,入院リスクや死亡率と比較することで維持透析患者におけるシステムの検証について述べる.
方法
患者
サンフランシスコ総合病院での外来慢性透析プログラムは研究期間中に91名の維持透析患者を治療した.選択基準は最低3ヶ月以上維持透析を経過した18才以上の患者だった.3名の患者は基準に合致しなかった.88名の登録患者のうち2名の患者が研究期間中に他の施設に入院し,3名の患者が参加に同意しなかった.それゆえ83名の患者(男性44名女性39名)がこの研究に参加することに同意した.本研究は治験審査委員会で承認され,全ての患者から書面で同意を得た.
従来の主観的包括的評価
栄養状態の主観的包括的評価 (SGA) は腎臓病においても一般的に用いられている通り,病歴と身体所見に基づく半定量的な採点システムである.病歴には5つの要素が含まれる.過去6ヶ月間の体重減少,消化器症状,経口摂取量,運動耐容能,合併症である.それぞれの機能は別々に A, B, C と点数化されており,良好な栄養状態から重度の低栄養のカテゴリまで対応する.身体所見には2つの要素が含まれる.皮下脂肪減少と筋委縮である.浮腫や腹水の出現はSGA原法の身体所見の3番目の要素であるが,透析患者には普通用いない.これら2つの要素は0点から3点に分類され,正常から極めて異常であることを示す.データは主観的に点数化され,患者は3つのSGA点数に分類される.Aは栄養状態良好,Bは軽度か中等度の低栄養,Cは重度の低栄養.透析患者におけるSGA評価方法の詳細は以前刊行された文献の巻末として利用でき,またAmerican Journal of Kidney Disease のウェブサイト上で利用可能である. //www.ajkd.org
Dialysis Malnutrition Score
従来の SGA の要素を用いて最近著者の一人が定量的採点システムである Dialysis Malnutrition Score (DMS) を開発した.それは SGA の7つの要素を含んでいる.体重変化,食事摂取量,消化器症状,運動耐容能,合併症,皮下脂肪,筋萎縮徴候である.腹水と浮腫は除外し,透析治療を何年間受けているか(透析歴)を合併症の要素に追加した.各々の要素は1点(正常)から5点(重度の異常)まで点数化した.そのため7つの要素の合計点素は7点(正常)から35点(重度の低栄養)までとなり,DMS が高いほどより重度の蛋白質エネルギー低栄養であることを示す.異なる患者集団を用いた横断研究によると,DMS は身体測定値と透析患者の栄養状態の検査データとに有意に相関するとの予備報告がある.
Malnutrition Inflammation Score
さらに包括的で定量的な採点システムを作るために7つの DMS の評価基準を改訂し,3つの要素を追加した.Body mass index (BMI) と血清アルブミンと総鉄結合能 (TIBC) である.さらに各要素の重症度を5段階から4段階に減らした.以前の研究で DMS の5段階評価はもはや使われていないことを我々は記述しているからである.そのため,Malnutrition inflammation score (MIS) は10の要素を持ち,それぞれが0(正常)から3(重度の異常)までの4段階の重症度を持つ.10の MIS の要素の合計点数は0(正常)から30(重度の低栄養)までであり,点数が高いほど低栄養と炎症の重症度が高いことを反映している.
Figure 1 に我々の採点用紙を掲載した.栄養歴,身体所見,BMI,検査結果の4つのセクションと10の要素からなる.病歴セクションは5つの要素が SGA 原法から採用された.体重変化は過去6ヶ月間浮腫のない透析後体重の変化と定義した.低い点 (0) は0.5 kg 未満の体重減少または体重増加の際に与えられる.1点は 0.5 kg 以上 1.0 kg 未満の体重減少に与えられる.2点は 1.0 kg 以上かつ体重の 5 % 未満の体重減少を示す.3点は5 % 以上の体重減少を示す.
経口摂取量について.通常固形物(形のあるもの)を食べ,最近摂食量の減少がない場合に経口摂取は0点と採点する.柔らかい固形物を食べている場合は1点と採点し,流動食のみの場合や摂食量が中等度減少している場合は2点と採点し,一日の摂取量が生命維持に不十分な状態が慢性的に続いている場合に3点と採点する.
消化器症状について.患者に食欲があり全く消化器症状がない場合は0点と採点する.軽度の食欲低下や軽度の嘔気がある場合は1点,時に嘔吐したり他の中等度の消化器症状がある場合(腹痛など)は2点,下痢や頻回の嘔吐,重度の食欲不振がある場合は3点と採点する.
運動耐容能について.正常な運動耐容能であるか,以前の耐用能低下から改善している場合は0点と採点する.平地歩行が軽度か時々困難である場合,頻回に疲労感を感じている場合は1点と採点する.自力活動が困難である場合は2点,軽労作が制限されるか寝たきりないし坐位のままの場合は3点である.
SGA 変法 (DMS) にあるように,合併症には透析歴(透析治療年数)が含まれている.時間的要素は低栄養と炎症の程度に影響するからである.そのため合併症は他の医学的疾病がなく患者が透析導入1年未満の場合は0点と採点する.主要な合併症 (MCCs) を除外した軽度の合併症の場合,または透析導入後1年以上4年以下の場合に1点と採点する.MCCs とは III 度や IV 度のうっ血性心不全,重度の冠動脈疾患,臨床的に明らかな後天性免疫不全症候群,中等度から重症の慢性閉塞性肺疾患,転移性悪性腫瘍のことである.MCCs のうち1つを含んでもよいが中等度の合併症か,透析期間が4年を超える場合は2点と採点する.MCCs のうち2つ以上を有する場合は3点と採点する.糖尿病については,以前合併症について言及されていない場合は合併症として数えなかった.その代わり糖尿病患者の予後が不良となりうる合併症については個別に検査した.
身体所見のセクションは2つの要素からなる.身体の4つの部位での皮下脂肪沈着により体脂肪蓄積は評価される.つまり眼下,上腕三頭筋,上腕二頭筋,胸部である.筋萎縮徴候は7つの部位により簡潔に得られる.つまり側頭部,鎖骨,肩甲骨,肋骨(肋間筋),大腿四頭,膝,骨間の筋である.これら2つの要素をそれぞれ0点から3点まで採点し,正常から重度まで表現し,他の項に該当する基準に基づく従来のSGA ガイドラインに応じて割り当てられる.
透析患者の死亡率の予測値であるため,我々は身長で調整した体重の機能を追加した.BMI は透析後体重 (kg) を身長の二乗 で除した比で身長で補正した体重を選択した.BMI は0点から3点までの4段階で採点し,それぞれ20以上,18以上19.99以下,16以上17.99以下,16未満に対応する.
で除した比で身長で補正した体重を選択した.BMI は0点から3点までの4段階で採点し,それぞれ20以上,18以上19.99以下,16以上17.99以下,16未満に対応する.
MIS の4番目のセクションは2つの検査値からなる.血清アルブミン値はしばしば末期腎不全患者における死亡率の強い予測因子となり,低アルブミン血症は蛋白摂取減少と同様,炎症(急性期反応)を反映している.総鉄結合能は血清トランスフェリン濃度を反映し,炎症や鉄の貯蔵変動で変化はするが,透析患者の栄養状態と有意に相関する.それゆえこれら2つの検査値は MIS の総得点の20%を占める(詳細は Fig 1 を参照のこと).
本研究では熟練した医師が身体測定前にそれぞれの患者を5分から15分で採点した.再現性を検証するために同じ医師に1週間後に1回目の MIS 評価を参照せずに15名の患者を選んで MIS 評価を実施させた.両者の間の相関係数 (r) は 0.91 であり,再現精度は良好と考えた.
身体計測
体重評価と身体計測は透析治療後5分から20分後に迅速に施行した.上腕二頭筋皮下脂肪厚と上腕三頭筋皮下脂肪厚 (TSF) は従来の皮下脂肪キャリパーで測定した.これについては別途説明する.上腕中央周囲径 (MAC) はプラスチックテープで測定した.すべての身体計測は1名の医師が連続して3回迅速に計測し,3回計測した値の平均値を最終結果とした.上腕中央筋周囲径 (MAMC) は以下の式で計算した.
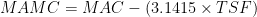
身長は患者カルテから得た.
近赤外分光方式
体脂肪率と除脂肪体重を評価するのに身体計測と同時に近赤外分光方式 (NIR) を実施した.商品化された NIR センサー (portable Futrex 5000) を用いた.近赤外分光値は Futrex センサーを各患者の非シャント上腕に置いて必要なデータ(性別,体重,身長,体格)を入力後数秒間で測定した.すべての患者の身体活動レベルは同程度と規定している.NIR で測定した体脂肪は維持透析患者において SGA や他の栄養評価と有意に相関することが報告されている.
入院
83名の全透析患者で12ヶ月間のこれらの測定が完了した後,在院日数データが得られた.在院日数とは一泊以上の病院への入院日数と定義した.入院当日は丸一日としたが,退院日は在院日数には数えなかった.それゆえ,在院日数の最小値は1日となった.除外基準は設けなかった.そして様々な疾病による在院日数を数えた.しかし,透析シャント関連の大部分の入院は一泊入院を要しないため,シャント関連の入院は他の合併症,例えば感染症や心血管合併症などを有することになった.研究を開始した時点で数名の患者が入院していたが最初の6ヶ月間は在院日数には数えなかった.1年間のコホート期間の最後にまだ入院していた患者については直前の入院の全期間を数えた.前向き12ヶ月間の追跡調査で9名の患者が死亡し,6名の患者がコホートから離脱し,生存期間の入院指数は12/生存期間(月数)で補正した.
12ヶ月間の前向き在院日数を臨床的予後として評価するため,3つの方法を使用した.年間入院頻度 (H1) は12ヶ月間の前向きコホート期間中の入院回数とし,先に定義したように個々の在院日数の長さは考慮しない.年間在院日数 (H2) は同じ期間中の全在院日数の合計とした.各個人ごとに1年間で,研究開始日からリスクが発生して初回入院に至るまでの日数を評価して生存モデルとした (H3) .併せて個人ごとのリスク期間を研究開始時点から最初の入院日か,打ち切りイベントか,研究開始1周年後の日までの日数と定義した.リスク期間は移植の3日前から切り捨てられた.移植治療のための入院を観察するのを回避するためである.
検査値
尿素除去比を計算するのに用いる透析後の血清尿素窒素を除いて,透析前の検査値は迅速に測定した.その際最後の鉄剤静注から最低でも16日空けた.血清CRPは炎症状態の指標として測定し,免疫比濁法によって測定した (Hitachi 747).CRP の最低感度は 6.9 ng/mL であった.CRP 値が 6.9 ng/mL 以下と報告された患者では,統計解析のため任意の平均値として 3.4 ng/mL を用いた.検査値は自動測定装置で測定した.すべての検査値は Spectra laboratories によって検査した.
透析と疫学手法
最初に83名の患者で横断研究を行い,その後12ヶ月間にわたって前向きコホート研究を行い,予後の連続変数としての入院データおよび二分化転帰としての死亡率を検証した.我々は Pearson の相関係数 r を連続変数間の選択分析として使用した.男性と女性の間の群間比較に Student-t 検定(両側)を使用した.Pearsonの相関係数 r は関連の有意性と強度を定義するのに用いた.Spearman の順位相関もまた SGA や人種,基礎疾患などのノンパラメトリック機能のような変数に用いた.そしてその結果は Pearson の r と比較した.多変量解析を行い,性別や年令,人種,腎疾患などで一部調整した相関係数を得た.
前向きコホート研究における最初の入院と死亡の相対危険度を計算するため,前述したように人口統計学的変数をコントロールとした Cox 比例ハザードモデルを用いてハザード比と95%信頼区間を得た.1.00 を含まない95%信頼区間は統計学的有意と考えられる.Cox 比例ハザードで計算した R2 は(pseudo-R2 としても知られるが)他の多変量相関係数と比較するのに用いられる.Y軸を生存率の対数の負とし,X軸に生存期間の対数をプロットした両対数グラフを描き,線形性の仮定が妥当であることを確立した.各々の多変量モデルは1つの予後変数(従属変数)と5つの予測変数(独立変数),年齢,性別,人種,基礎腎疾患,およびその特定のモデルごとの変数を含んでいる.それゆえ,一般的な Cox 回帰のための多変量モデルは以下の式となる.
![\displaystyle\lambda(t)=\lambda_{0}(t)[exp(b_{1}age+b_{2}sex+b_{3}race+b_{4}disease+b_{5}X)] \displaystyle\lambda(t)=\lambda_{0}(t)[exp(b_{1}age+b_{2}sex+b_{3}race+b_{4}disease+b_{5}X)]](https://s0.wp.com/latex.php?latex=%5Cdisplaystyle%5Clambda%28t%29%3D%5Clambda_%7B0%7D%28t%29%5Bexp%28b_%7B1%7Dage%2Bb_%7B2%7Dsex%2Bb_%7B3%7Drace%2Bb_%7B4%7Ddisease%2Bb_%7B5%7DX%29%5D&bg=T&fg=000000&s=0)
 は推定危険度であり,t はイベントか検閲までの時間であり,b1 から b5 まではモデルの項の係数である.X は前述した変数であり,MIS の結果やその要素,他の変数(SGA, DMS, BMI, NIR で測定した体脂肪,Kt/V や患者の検査値)を含む.それゆえ各々の予測変数と転帰(最初の入院や死亡)との間の関連は独立した多変量モデルを用いて研究した.ただし各々のモデルに均一なケースミックス調整を用いて.
は推定危険度であり,t はイベントか検閲までの時間であり,b1 から b5 まではモデルの項の係数である.X は前述した変数であり,MIS の結果やその要素,他の変数(SGA, DMS, BMI, NIR で測定した体脂肪,Kt/V や患者の検査値)を含む.それゆえ各々の予測変数と転帰(最初の入院や死亡)との間の関連は独立した多変量モデルを用いて研究した.ただし各々のモデルに均一なケースミックス調整を用いて.
統計ソフトウェアの Stata 5.0 を用いて記述統計と多変量統計を施行し,結果は全て2番目の統計ソフト Statistica for Windows 5.1 で検証した.限界基準は平均値±標準偏差で得られた.P 値が 0.05 未満は統計的有意とし,P 値が 0.05 と0.10 の間はわずかに有意とし,P 値が 0.10 より大きい場合は有意でないとした.
結果
Table 1 に臨床データ及び検査値を列挙した.年齢は22才から87才まで(55.8歳±15.3歳),透析歴(慢性透析治療期間)は4ヶ月から12年まで(43ヶ月間±33ヶ月間)だった.理想体重(69.1kg±19.6kg)は透析直後の浮腫のない体重の平均値である.透析間の体重増加は 1.74 kg ± 0.56 kg であった.4名の患者はエリスロポエチンが不要であった.残りの患者はエリスロポエチンの静注投与を受けており,週に3000単位から36000単位まで(7928単位±7730単位)であった.78名の患者が鉄剤 (200mg/月) の投与を持続的に受けており,他の患者は鉄剤を経口的に内服処方されていた.女性は男性より平均で11歳年齢が上であった.皮下脂肪測定,体脂肪率,Kt/V は女性のほうが高く,MAMC,除脂肪体重,血清クレアチニン値は男性のほうが高かった.3つの採点システム (SGA, DMS, MIS) では男女間の差異は有意ではなかった.
Table 2 に3つの栄養採点システムの相関係数および関連する変数を示す.3つの栄養採点システムの中では MIS が入院を予測するのに最も強力であった(調整相関係数は在院日数で 0.45, 入院頻度で 0.46).SGA は皮下脂肪厚,MAC,体脂肪率により強く相関する傾向があった.皮下脂肪計測と体脂肪では DMS と MIS のどちらも近い相関があったが,上腕計測や除脂肪体重,BMI では MIS がより強い相関を示した.ほとんどすべての検査値では MIS が SGA や DMS と比較してより強い相関を示した.血清クレアチニン値とヘマトクリット値は SGA と DMS では有意な相関はなかったが,MIS では有意に相関していた.このことは低栄養の維持透析患者は MIS 値が高いほど血清クレアチニン値が低く重度の貧血であることを示唆している.しかしながら,MIS には既に2つの検査値を内包していることを改めて表明しておく必要がある.それゆえ,MIS とそれらの検査値との相関は少なくとも一部は数学的共役(多重共線性?)であることが予想される.血清 CRP 値は DMS とは相関せず,SGA に弱い相関が見られたのみであった.しかし CRP 値は MIS とは強い相関 (r = 0.41; P < 0.01) が見られた.このことは MIS が重症度だけでなく炎症の程度をも反映していることを示唆している.3つの栄養採点システムは全て年齢と正の相関を示した.これは高齢の患者ほどより重症の蛋白質エネルギー低栄養と炎症を有する傾向があることを示している.アルブミン,BMI,そして恐らくトランスフェリンも透析予後を規定すると報告されているため,我々はこれらの値を MIS と比較することを選出した.我々は相関方法は少なくとも数学的共役の一部であることを認めていたのだが.
Table 3 に多様な様々な対策の相関係数と入院頻度を示した.この表にそれらの値のみ記載した,どの入院頻度とも有意に相関する係数を少なくとも1つ示している値を.血清アルブミン値は MIS のそれよりわずかに大きな相関係数を持つ唯一の値だった.血清 CRP,コレステロール,フェリチン,クレアチニン値もまた入院頻度に対して統計的有意であった.MIS に対するアルブミンほど強くはなかったが.
12ヶ月間の観察期間中に9名の患者が死亡した(平均死亡経過月数は 6.9 ± 2.7 ヶ月).6名の患者がコホートから離脱した,3名の患者は腎移植を受け,2名の患者は透析方法を腹膜透析に変更し,1名の患者は他の場所へ引越していった.46名の患者がこの期間中に少なくとも一回は入院した.
Table 4 に前向きコホート研究の開始時の初期値と最初の入院までの時間 (H3) に基づく Cox 比例ハザードモデルによる最初の入院のハザード比と95%信頼区間を示す.そのモデルは年令,性別,人種,基礎腎疾患を調整して相対危険度を推定した.Table 4 には統計的に有意な (P < 0.05) 相対死亡危険度のみ示した.3つの採点システムの中では MIS が H3 と最も強く相関していた.最初の入院の相対危険度は MIS が 3.83 上昇すると10単位増加した(95%信頼区間は 1.85 から 7.94; P < 0.001).DMS は弱い相関しかなかった.他の変数では血清アルブミン値が H3 の強い予測因子となった(ハザード比 4.48; 95%信頼区間 2.16-9.28; P = 0.001).血清 CRP もまた H3 と統計的に有意な関連を示した.血清クレアチニンは僅かな関連のみだった.Cox 比例ハザードモデルでは,他のすべての臨床変数・検査値変数・図示した変数は H3 とは統計的有意な関連は示さなかった.
Table 5 には H3 について先述したのと同様 Cox 比例ハザードモデルを用いて死亡のハザード比と95%信頼区間を示した.統計的有意な相対死亡危険度の値のみ Table 4 に示した.ただしここで述べておくが,他の採点システムと比較してDMS は除外してある(P = 0.06).3つの採点システムの中では MIS が最も強く前向き死亡率と関連していた.MIS が 10.43 増加すると相対死亡危険度は10単位増加した(95%信頼区間 2.28 から 47.64; P = 0.002).SGA には弱い関係しかなく,DMS には統計的に有意なハザード比はなかった.他の変数では,血清アルブミン値もまた死亡の強い予測因子となった(ハザード比 7.21; 95%信頼区間 2.47 から 11.74; P = 0.001).血清 CRP,コレステロール,クレアチニンもまた年間死亡率と統計的に有意な関連を示した.他のすべての臨床データ,検査値,図示した変数は Cox 比例ハザードモデルによる死亡率とは統計的有意な関連を示さなかった.
Table 6 にはMIS の10の要素と MIS 値とに対する最初の入院と死亡のケースミックス調整したハザード比を示した.MIS の各要素を前述したように0から3まで増加する変数として Cox モデルに入力した.6つの MIS の要素は最初の入院 (H3) のハザード比に対して統計的有意を示し,5つの MIS 要素は死亡に対して統計的に有意なハザード比を示した.皮下脂肪と筋委縮に対する主観的点数が H3 に対して最も強い関連を示し,皮下脂肪と運動耐容能は死亡に対して最も強い関連を示した.しかし MIS 値は H3 と死亡率に対しては10個のどの要素よりももっと強力であることが分かった (Table 6).
Table 7 には DMS のオリジナルの7つの要素に対して付加的な3つの要素であるアルブミン,TIBC,BMIに基づく MIS モデルの逐次展開を示した.最初の列は(多変量解析して)ケースミックス調整した死亡のハザード比の相関係数 R2 を示す(Cox 比例ハザードモデルでは pseudo-R2 として知られる).その後の列には入院指数 (H1 から H3 まで) の多変量 R2 ,血清 CRP 値,ヘモグロビン値,MAMC,MIR 体脂肪率が多変量線形回帰モデルに基づいて示してあるが,最初の入院 H3 は除外してある.Cox モデルに基づく死亡ハザード比に近接しているためである.最初の7つの行は,最初の7つの要素 (DMS*) に対して以前言及した要素(アルブミン,TIBC,BMI)のうち一つかそれ以上の付加要素に基づく採点システムのモデルの様々な組み合わせを示している.8番目の行は MIS のフルバージョンであり,(*で示した)DMS と3つの付加要素である.9行目はアルブミンを CRP で置き換えた採点モデルを示す.MIS では H3 と死亡のハザード比が最強である.3つの新しい要素を追加することで死亡率のベストの指標を作ることが正当化される.TIBC を欠いたモデルが入院頻度 (H1 と H2) と体脂肪率に僅かな相関しかないとしても,MIS は H3 と死亡率のハザード比においてだけでなく,CRP 値,ヘモグロビン値,MAMC との強い相関を考慮しても,まだ上回る.MIS は近赤外分光方式で測定した体脂肪率とは最も強く相関してはいなかったが,MAMC との相関を考慮すると最も良い予測モデルであった.
Table 7 において9番目のモデルはアルブミンを CRP で置き換えたもので,MAMC,MIR 体脂肪,そしてもちろん CRP とより強い相関を示した.しかし死亡ハザード比,全ての3つの入院指標,ヘモグロビン値はそれほど強くなかった.それゆえ CRP ではなくアルブミンを用いたオリジナルの MIS がより有用と判明した.他のモデルも作成して検証してみたが,例えば CRP 値を10個の要素に追加して11個の要素にするなど,大部分の相関係数が改善すると期待されたにも関わらず増加はごくわずかであった(データは示さない).さらに CRP は多くの医療機関においてはいつも測定する検査項目ではない.それゆえ,一般には MIS が炎症指標や身体測定値,貧血同様に全体的な予後とよく相関する最良のモデルであると分かった.
考察
従来の SGA の要素に BMI と2つの検査値を結合して我々は定量的で包括的な MIS を開発した.それは簡易で実用的,再現性があり,もっと客観的に低栄養と炎症を評価する方法である.MIS は包括的な採点方法であり,前向きの入院指数,死亡率,栄養や炎症・貧血の代理と有意な強い相関を持つ.維持透析患者の栄養と炎症を評価することと個人ごとの重度の罹患率や致死的イベントの高いリスクを同定することの評価が信頼できると分かった.
低栄養と炎症は維持透析患者には一般的に起こることであり,不良な臨床状態やこの患者群における更に悪い予後と MICS が関係しているとはまだ十分に定義されていない.それにもかかわらず,透析患者の栄養と炎症の統一した評価方法がない.よく知られた身体測定から精巧な技術を用いたものまで,いくつかの低栄養の指数が利用できる.例えば二重エネルギーX線吸収法など.しかし,蛋白質エネルギー低栄養を検出するその方法の信頼性と実用性に説得力はない.さらに,透析患者の中で炎症状態を測定する方法はよく研究されておらず,種々のサイトカインをより精巧に測定する方法は高価で,まだ議論のあるところであり,利用するにも研究施設により制約される.
SGA は簡便で信頼できるツールであり,栄養状態を検出し疾病の程度を予測することが検証されたにも関わらず,それはたった3つの栄養状態を含んだ半定量的採点法である.この半定量的機能は SGA の信頼性と精度を制約する.さらに SGA の殆どの要素は明確な定義を持たないために強固なガイドラインは存在し得ない.それゆえ SGA の基準の各々の最終的評価はもっぱら評価者の主観に頼らざるをえない.
SGA の最初の定量的バージョンは DMS であるが,SGA に固有の問題を回避しようとした正当なものである.DMS は TIBC や血清アルブミン値同様,身体指数と BMI に良好な相関を示した.予備データは DMS が SGA よりよい精度を提供することを支持していたが,我々はツールを改善する努力を続けた.目的は,栄養士や熟練した看護師,または医師が数分以内でもっと簡単に実施できる実用的で簡便な採点方法である.しかしそれは包括的である必要があり,歴史の境界を超える必要があり,SGA や DMS をより簡便化した診察方法である必要があり,また内的な炎症を反映し,死亡率や入院など臨床に関連する転帰を予測可能である必要があった.
MIS は SGA に基づいてはいるが SGA にはない3つの要素,つまり BMI,血清アルブミン,TIBC を持っており,加点方式(0点から3点までの増加する整数)で採点する.そしてその点数は他の既に存在する SGA や DMS の7つの要素と互換性がある.MIS と血清アルブミン (- 0.51) およびトランスフェリン (- 0.42) に対する交差相関は DMS に対するもの(それぞれ – 0.27, – 0.23)より強かった.これら2つの検査値が MIS の要素だからでもある.我々は BMI を身長で補正した体重の簡便な代表値として用いたが,透析患者の死亡率を予測することが分かった.血清アルブミン値は透析患者の死亡率のより強い予測因子であるが,低アルブミン血症は低栄養同様,炎症を反映している可能性がある.血清トランスフェリンは TIBC により代表され,米国の透析施設では毎月から四半期ごとに採血するもので,透析患者の栄養指標として信頼できると報告されている. BMI,アルブミン値,トランスフェリンの3つの付加要素は MIS の総得点の一部を構成していることで数学的共役の懸念はあるが,その利点は相当なものであり,数学的共役を超えている.
前向き入院と有意に相関する MIS は,維持透析患者の死亡の予測因子でもあることが分かった.疑いもないことだが,MIS と罹患率および死亡率の相関は改善した.少なくとも血清アルブミン値や BMI などのよく知られたマーカーを包含するという理由で.それが MIS に含まれる理由なのだが.
MIS と CRP の相関が強い(r = 0.41) のは,血清アルブミンが MIS の要素であり,アルブミンが CRP と強く相関することが知られているためだろう.DMS は本質的に SGA の定量的バージョンであるにもかかわらず,CRP とは統計的に有意な相関を示さなかった (r = 0.19).また SGA と CRP の間の相関は弱かった (r = 0.24).それゆえ,MIS が低栄養同様炎症のマーカーであり,MICS の重症度の指標であることが分かった.
SGA や DMS と異なり,MIS は不応性貧血のマーカーであることも分かった.MIS とヘマトクリットの間に優位な相関が見られ,恐らく炎症と維持透析患者のエリスロポエチン抵抗性との間に関連があるためだろう.Gunnell らはエリスロポエチン抵抗性は高フェリチン血症と低トランスフェリン血症の文脈で起こり,急性反応期にあると考えられ,鉄欠乏状態ではないと報告している.さらに低 TIBC 血症と高フェリチン血症は透析患者の罹患率・死亡率を高める危険因子である.これらの所見は,我々が MIS に血清 TIBC(トランスフェリン)を含んだことをさらに支持する.
本研究では,期待したとおり,血清アルブミンもまた前向き入院指数と死亡率に強い相関があることが分かった.しかし MIS は予後に近く相関するだけでなく身体所見や貧血・炎症・栄養指標などの検査値にもより強い相関を示していた.他の多くの検査値と臨床状態を特徴付けるのに使われる臨床測定で,異なる測定が所与の疾病の異なる面を記述するかもしれないし,互いによく相関しないかもしれない.それゆえ,血清アルブミン値と身体測定値との間の強い相関がないのは珍しいことではない.血清アルブミン値が MIS の要素であることは強調されるべきかもしれない.それゆえ,数学的共役がアルブミンと MIS の間の相関に貢献しているはずである.にも関わらず MIS の 90 % が他のアルブミンには関係のない変数である.MIS とすべての関連する臨床指標の平均的な相関はアルブミンや CRP,他のいかなる変数のそれを超えている.それゆえ,MIS は透析患者の栄養と炎症のすべての面を反映するより包括的なマーカーであり,同時に維持透析患者の罹患率と死亡率の強い予後規定因子であることが分かった.
予備調査の結果は標本数と観察期間が小さすぎることで修飾されているはずである.さらに,重病のため本研究に参加しなかった2名の患者が研究開始直後に死亡した.MIS 値が非常に高かったため,もしその患者が参加していれば入院率と死亡率についてはより強い結果が得られた可能性がある.さらに透析歴の効果は我々が使用する MIS の単純な増分の効果よりもっと複雑かもしれない.また,BMI の加点方式(20超は正常)は厳しすぎて歪んでいる可能性がある.というのも BMI の平均値は 24.7 ± 6.4 kg/m2 だからだ.それゆえ, 60 % 以上の患者が正常と採点された.にも関わらずこれら全ての点数はヌルに対する偏りを示し,これらの基準を改善することで更に良い相関を期待できることを暗示している.
本研究で検証した採点方法では殆どの相関は特に堅牢でもなかったことを強調しておく必要がある.疑いもないことだが,例えば低栄養炎症複合状態などの複雑な生理的状態にあるものを測定する基準を作成してスケールの方法を開発するのは,技術的に洗練され過ぎており,非定型的アプローチを保証するとは最初は思えなかった.しかしながら,本研究の目的は新しい採点方式を創造することではなく,SGA のような既に存在するものを洗練して検証することである,ということは改めて強調しなければならない.臨床に関連した低栄養スケールを開発することは努力を必要とし,SGA は良いスタート地点であった.SGA は予測と内容の有効性を有しており,栄養リスクのベンチマーク測定としてますます受け入れられている.そして MIS は本質的に SGA ベースでその要素を 70 % 有しており,30 % は3つの付加要素(アルブミン値,トランスフェリン値,BMI)からなる.それらはしばしば検証され,透析患者における栄養状態のマーカーとして一般的に受け入れられている.
透析患者の予後不良の2つの主要な指標である栄養と炎症を評価する目的は,合併症と予後不良のリスクのある患者を同定することである.そのようなリスク層別化戦略は伝統的に二桁の採点方式に基づいているが,追加の栄養カウンセリングや栄養サプリメント,心理社会的介入などの予防介入の実施を可能にする.この開発された MIS には SGA と DMS の利点,つまり広く用いられている信頼性,精度,3つの要素を追加するだけの強度などが組み込まれており,それらは全て透析の予後に軸受している.取り組む時間とスタッフの訓練は増えない.
Dialysis Outcome Quality Initiative ガイドラインでは,すべての患者に統一した栄養評価を定期的に行うことを推奨している.栄養と炎症状態の全体的測定に対する注意を増すことは患者の予後を改善するようである.この仮説は透析患者の観察コホートやランダム化コントロール試験によって検証されるべきである.そのような介入が為される前に標準化した統一した一般的に受け入れられた栄養と炎症の評価方法を採用すべきである.あまねく使われて十分実用的で,しかも予後の強い予測因子として十分に包括的なツールを.MIS はその目的達成のための手段かもしれない.現在の研究は MIS が従来の SGA や DMS よりも優れている可能性があることを示唆している.とはいえ,MICS の存在と重大性を検出する採点方式と,透析患者の罹患率と死亡率の予測値との信頼性を評価するにはさらに包括的な縦断研究が必要である.


